Acyloïne

De acyloïnes (ook: ketol) vormen een groep van organische verbindingen, waarbij in de α-positie van een carbonylgroep een hydroxylgroep is geplaatst. Daarom worden het ook wel α-hydroxycarbonylverbindingen genoemd.
Door de aanwezigheid van een hydroxylgroep naast de carbonylgroep is er mogelijkheid tot stabilisatie door middel van waterstofbrugvorming.
Synthese
Er bestaan enkele klassieke reactiemethoden om acyloïnes te synthetiseren:
- De acyloïnecondensatie: een reductieve koppelingsreactie van esters
- De benzoïnecondensatie: een condensatiereactie tussen 2 aromatische aldehyden
- De Rubottom-oxidatie: de oxidatie van een silylenolether met 3-chloorperoxybenzoëzuur
- De oxidatie van carbonylverbindingen met dizuurstof (deze reactie is echter weinig selectief)
- De zogenaamde MoOPH-oxidatie van carbonylverbindingen met molybdeenperoxide, pyridine en hexamethylfosforamide
Reacties
De reductie van een acyloïne levert een vicinaal diol, terwijl de oxidatie vicinale diketonen levert.
Een specifieke reactie is de Voight-aminering, waarbij een acyloïne met een primair amine en fosforpentaoxide reageert tot een α-keto-amine:[1]
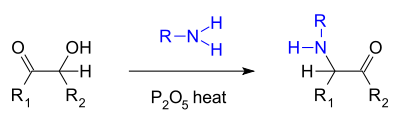
De Voight-aminering.
Bronnen, noten en/of referenties
- ↑ (en) E. von Meyer, Karl Voigt (1886) - Ueber die Einwirkung von primären aromatischen Aminen auf Benzoïn, Journal für Praktische Chemie, 34 (1), pp. 1–27











