Ikatan tiga-pusat dua-elektron
Ikatan tiga-pusat dua-elektron merupakan sejenis ikatan kimia yang kurang elektron, di mana tiga atom saling berbagi dua elektron. Kombinasi tiga orbital atom membentuk satu orbital ikat, satu orbital anti ikat, dan satu orbital non-ikat. Dua elektron berada pada orbital ikat, menghasilkan efek ikatan secara keseluruhan dan merupakan ikatan kimia yang mengikat tiga atom tersebut. Pada kebanyakan ikatan sejenis ini, orbital ikat berpusat pada dua atom daripada secara merata tersebar pada tiga atom. Contoh paling sederhana ikatan 3c-2e adalah ion H3+ ion.[1]
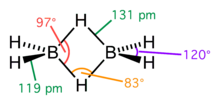
Ikatan sejenis ini banyak terlihat pada senyawa boron, seperti diborana, B2H6; monomer senyawa ini, BH3, tidak stabil karena atom boron dikelilingi oleh enam elektron valensi, sehingga untuk membentuk oktet, ia berbagi elektron dengan ikatan B-H atom boron lainnya, membentuk ikatan 3-pusat-2-elektron B-H-B. Pada borana, terdapat dua ikatan berjenis ini: dua atom H menjembatani dua atom B dengan sisa dua atom H merupakan ikatan B-H yang biasa. Pola ikatan ini juga dapat dilihat pada trimetilaluminium (Al(CH3)3), di mana atom karbon dari gugus metil menjembatani. Jenis ikatan ini juga muncul pada senyawa karbon, yang kadang-kadang dirujuk sebagai hiperkonjugasi;.
Penataan ulang karbokatium terjadi selama keadaan transisi ikatan tiga pusat. Karena struktur ikatan tiga pusat memiliki energi yang hampir sama dengan karbokatium, umumnya hampir tidak ada energi aktivasi yang dibutuhkan sehingga penataan ulang ini dapat terjadi dengan laju yang sangat cepat.
Apa yang disebut sebagai karbokation non-klasik memiliki ikatan tiga-pusat dua-elektron. Contohnya adalah kation norbonil.
Lihat pula
- Ikatan tiga-pusat empat-elektron
Referensi
- ^ "IUPAC Gold Book" (PDF). Diarsipkan dari versi asli (PDF) tanggal 2007-06-10. Diakses tanggal 2009-02-06.
- l
- b
- s
| Ikatan kovalen & Antiikat | Ikatan sigma: 3c-2e · Ikatan pisang · 3c-4e (Ikatan hidrogen, Ikatan dihidrogen, Interaksi agostik) · 4c-2e Ikatan pi: Pengikatan balik π · Konjugasi · Hiperkonjugasi · Aromatisitas · Aromatisitas logam Ikatan delta: Ikatan rangkap empat · Ikatan rangkap lima · Ikatan rangkap enam Ikatan dipolar · Haptisitas |
|---|---|
| Ikatan ion | Interaksi kation-pi · Jembatan garam |
| Ikatan logam | Aromatisitas logam |
| Ikatan hidrogen | Ikatan dihidrogen · Kompleks dihidrogen · Ikatan hidrogen sawar rendah · Ikatan hidrogen simetris · Hidrofil |
|---|---|
| Nonkovalen lain | Gaya van der Waals · Ikatan mekanis · Ikatan halogen · Aurofilisitas · Interkalasi · Penumpukan · Gaya entropik · Polaritas kimia |









