Tiosyanaatti

Tiosyanaatti eli rodanidi on negatiivisesti varautunut ioni eli anioni, ja epäorgaaninen yhdiste. Tiosyanaatit ovat tiosyaanihapon (HSCN) eli vetyrodanidin suoloja. Tiosyanaatin kemiallinen kaava on [SCN]−. Lähes samankaltainen ioni on syanaatti-ioni, [OCN]−, jossa rikkiatomin tilalla on happi. Nimi rodanidi juontuu kreikan kielestä ja perustuu rautatiosyanaatin punaväriin.
Myrkyllistä kahdenarvoista elohopeatiosyanaattia on joskus käytetty pyrotekniikassa, mutta sen myrkyllisyyden vuoksi tästä on pitkälti luovuttu.
Rodanaasi-entsyymi muuntaa kehossa rajatussa määrin myrkyllistä syanidia, CN−, vähemmän vaaralliseksi tiosyanaatiksi.[1]
Rauta(III)- ja koboltti(III)-ionien osoitusreaktiot
Lisäämällä tiosyanaattia (esim. ammoniumtiosyanaattina) vesiliuokseen, voidaan liuoksessa mahdollisesti olevat rauta(III)-ionit havaita. SCN- nimittäin muodostaa Fe3+ kanssa vesiliuoksissa helposti havaittavan verenpunaisen hydratoituneen koordinaatiokompleksin [Fe(SCN)]2+, jonka tarkempi rakenne on [Fe(SCN)(H2O)5]2+. Osoitusreaktiossa muodostuu myös pienempiä määriä muita hydratoituneita komplekseja kuten Fe(SCN)3 ja [Fe(SCN)4]−.[2]
-
![Yleisin reaktiotuote, [Fe(SCN)(H2O)5]2+](//upload.wikimedia.org/wikipedia/commons/thumb/1/11/Pentaaquathiocyanatoiron%28II%29-3D-balls.png/120px-Pentaaquathiocyanatoiron%28II%29-3D-balls.png) Yleisin reaktiotuote, [Fe(SCN)(H2O)5]2+
Yleisin reaktiotuote, [Fe(SCN)(H2O)5]2+ -
 Reaktiotuoteseoksen väri
Reaktiotuoteseoksen väri
Liuosten koboltti(III)-ionit voidaan havaita samalla tapaa, sillä tiosyanaatti muodostaa niiden kanssa sinisiä hydratoituneita komplekseja.[3]
Tiosyanaatteja
- Ammoniumtiosyanaatti NH4SCN, CAS-numero 1762-95-4
- Elohopeatiosyanaatti Hg(SCN)2, CAS-numero 592-85-8
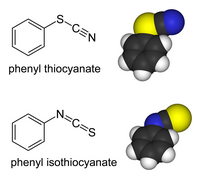
- Fenyylitiosyanaatti C7H5NS, CAS-numero 5285-87-0
- Kaliumtiosyanaatti KSCN, CAS-numero 333-20-0
- Metyylitiosyanaatti CH3SCN, CAS-numero 556-64-9
- Natriumtiosyanaatti NaSCN, CAS-numero 540-72-7
- Rautatiosyanaatti Fe(SCN)3, CAS-numero 4119-52-2
Lähteet
- ↑ M Libiad, A Sriraman, R Banerjee: Polymorphic Variants of Human Rhodanese Exhibit Differences in Thermal Stability and Sulfur Transfer Kinetics. The Journal of Biological Chemistry, 25.9.2015, 290. vsk, nro 39, s. 23579–23588. PubMed:26269602. doi:10.1074/jbc.M115.675694. ISSN 0021-9258. Artikkelin verkkoversio.
- ↑ NN Greenwood: Chemistry of the elements, s. 1090. 2. painos. Butterworth-Heinemann, 1997. ISBN 0750633654.
- ↑ N Uri: The stability of the cobaltous thiocyanate complex in ethyl alcohol-water mixtures and the photometric determination of cobalt. Analyst, 1.1.1947, 72. vsk, nro 860, s. 478–481. doi:10.1039/AN9477200478. ISSN 1364-5528. Artikkelin verkkoversio.
Aiheesta muualla
- IUPAC Gold Book: Thiocyanates (englanniksi)
![Yleisin reaktiotuote, [Fe(SCN)(H2O)5]2+](http://upload.wikimedia.org/wikipedia/commons/thumb/1/11/Pentaaquathiocyanatoiron%28II%29-3D-balls.png/120px-Pentaaquathiocyanatoiron%28II%29-3D-balls.png)











